Búsqueda
Búsqueda Avanzada
de Fármacos
Anatomía
A tener en cuenta:
- Lista de Carcinógenos por el IARC (Agencia internacional de investigación del cáncer)
- Cáncer y Medio Ambiente por ANSES (Agencia nacional de seguridad sanitaria francesa)
- Oncogenes
- Epigenética y Cáncer
- Resistencia a drogas mediada por la glicoproteína P
- Vacunas terapéuticas en cáncer
- Factores de Crecimiento y Citocinas
- Apoptosis: muerte celular programada
- Receptores de superficie celular
Teoría Básico
Cánceres más visitados
31585
Leucemia linfoblástica aguda
18206
Cáncer tiroideo
16237
Tumor de células germinales extragonadal
15698
Cáncer de vejiga
15087
Fármacos más visitados
30828
Yodo radiactivo (I-131)
20484
Hipertermia magnética por nanopartículas
17457
Denosumab
16842
Bicalutamida
15769
Novedades Fármacos/Tratamientos
Últimos comentarios
Megestrol acetato
Estoy en Búsqueda del medicamento Acetato de Megestrol Muchas gracias Estoy atento a cualquier... Mario
Mesotelioma pleural maligno
Hola José. Lo que le han hecho son tratamientos paliativos porque realmente no tiene cura, puede... Jose
Mesotelioma pleural maligno
Dear Dr. I have afriend with this desease and as far as I know there is contact with asbestos or... Rebeca
Histiocitoma fibroso maligno óseo
Este medicamento funcionaria para un adulto de 86 años. Gracias... NEMESIO
Ciproterona
llevo 9 meses tomando androcur 30 mg.mis senos han crecido siento piquete y se ha despertado el...
Tipo: Inmunoterapias
En este grupo se incluyen todos aquellos medicamentos capaces de estimular el sistema inmune del propio paciente para que éste sea capaz de reconocer y combatir las células enfermas. Algunos expertos los consideran una forma diferente de tratamiento al margen de la quimioterapia. La primera evidencia de 'inmunoterapia' data de finales del siglo XIX, en 1892, cuando William Cloey, un cirujano neoyorquino apreció una regresión espontánea del sarcoma entre aquellos de sus pacientes que habían padecido previamente una infección bacteriana.
Categoría: Inhibidores de los puntos de control inmunitario
Otros tipos de anticuerpos monoclonales mejoran su sistema inmunitario inhibiendo o deteniendo los puntos de control inmunitarios. El organismo utiliza los puntos de control inmunitario para detener de forma natural la respuesta del sistema inmunitario de atacar las células sanas. Las células cancerosas pueden hallar formas de esconderse del sistema inmunitario mediante la activación de estos puntos de control.
Los inhibidores de los puntos de control inmunitario evitan que las células cancerosas bloqueen el sistema inmunitario. Los puntos de control frecuentes que afectan estos inhibidores son las vías PD-1/PD-L1 y CTLA-4.
Diana:PD-L1
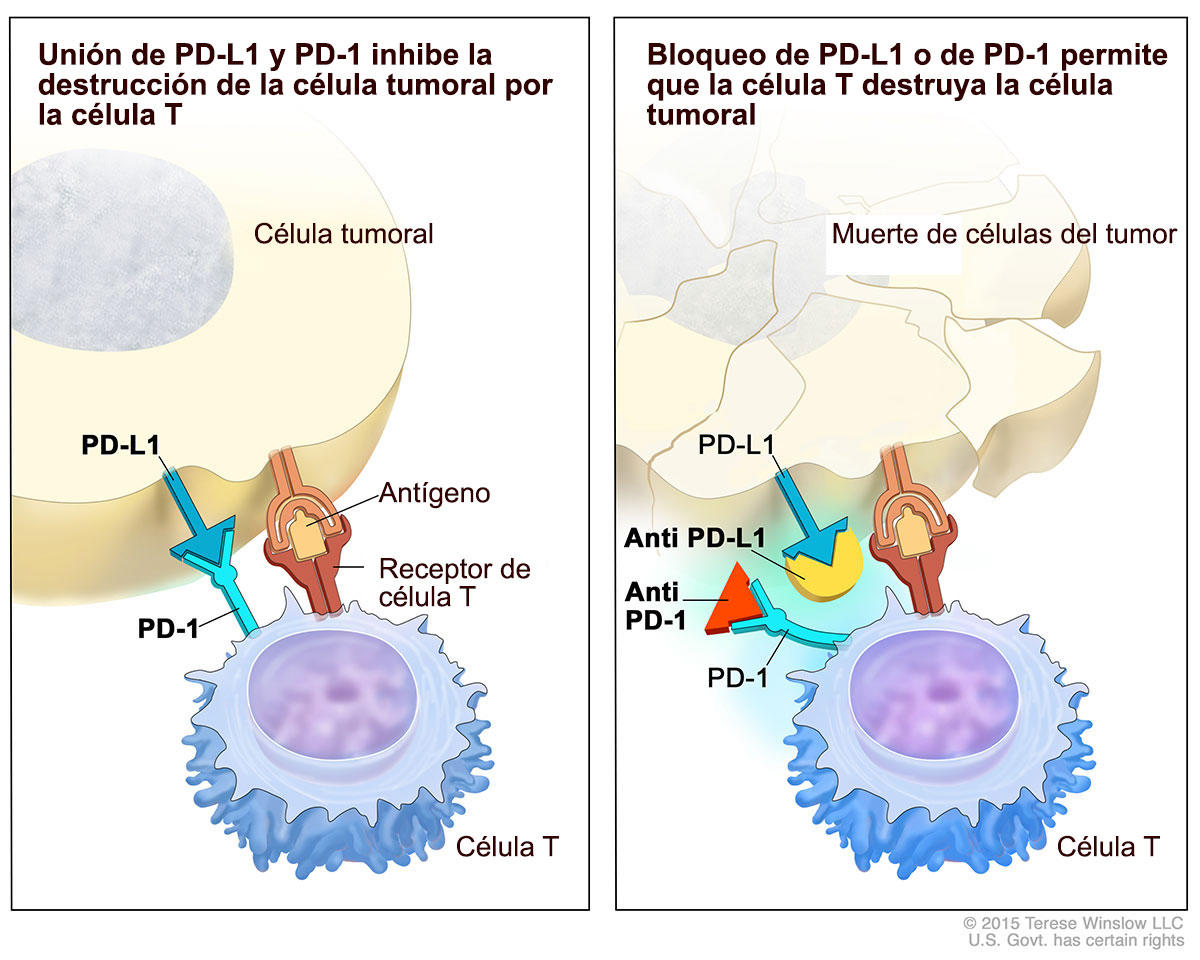
Proteína que actúa como un "freno" que controla las respuestas inmunitarias del cuerpo. Se encuentra PD-L1 en algunas células normales, y está en cantidades más altas que lo normal en algunos tipos de células cancerosas. Cuando PD-L1 se une a otra proteína que se llama PD-1 (proteína de las células T), no permite que las células T destruyan las células que contienen PD-L1, como las células cancerosas. Los medicamentos contra el cáncer llamados inhibidores de puntos de control inmunitario se adhieren a PD-L1 e impiden que esta proteína se una a PD-1. Esto libera los “frenos” del sistema inmunitario, lo que permite que las células T destruyan las células cancerosas.Nombre:
Atezolizumab
Comercial:
Tecentriq ®
Estado: Aprobado
Tratamientos aprobados por los diferentes organismos públicos y agencias de regulación sanitarias.
Tecnología: Anticuerpo Monoclonal

Foto:
Fórmula:
Gráfico:
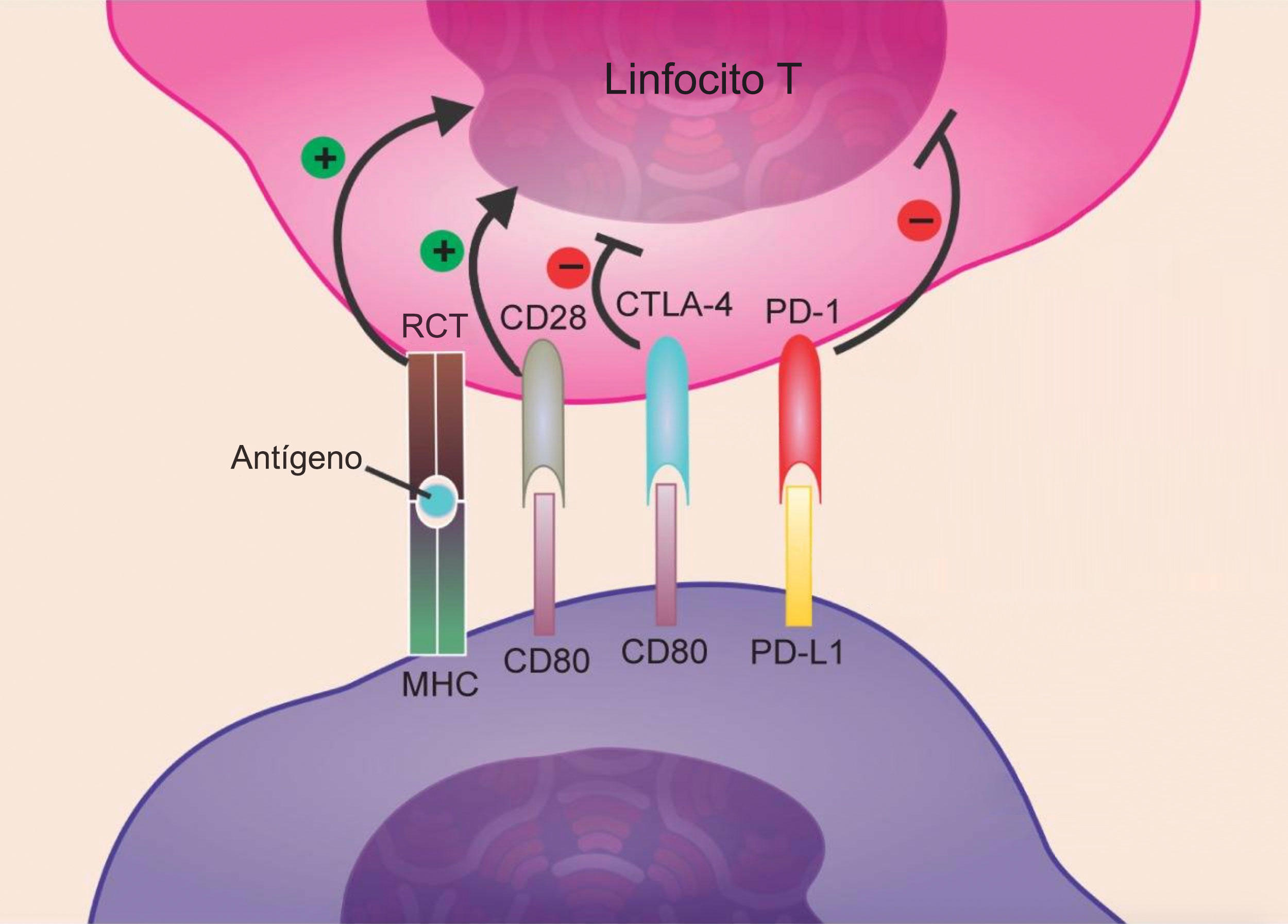
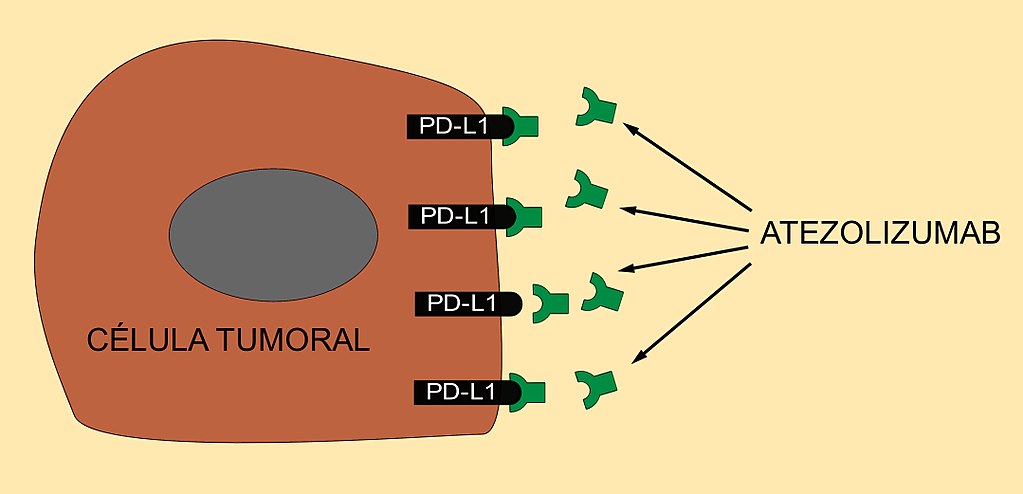
Información: Atezolizumab es un medicamento que pertenece a la familia de los anticuerpos monoclonales. Se ha sintetizado mediante técnicas de ingeniería genética y va dirigido contra la proteína PD-L1 (receptor de muerte programada 1). Está indicado para el tratamiento de determinados casos de cáncer de pulmón y cáncer del tracto urinario. Se vende con el nombre comercial de Tecentriq.
Mecanismo de acción
El incremento de la expresión de PD-L1 es uno de los mecanismos que permiten a los tumores malignos escapar del ataque del sistema inmunitario. En algunos tipos de cáncer como el carcinoma renal, los niveles de expresión de PD-L1 se correlacionan con la agresividad del mismo.
Atezolizumab es un anticuerpo monoclonal que bloquea los antígenos PD-L1 de las células cancerígenas y evita que ejerzan un efecto inhibidor sobre el sistema inmunitario, impidiendo su unión a los PD-1 del linfocito T.
https://es.wikipedia.org/wiki/Atezolizumab
El atezolizumab, que se vende bajo la marca Tecentriq, es un medicamento de anticuerpos monoclonales que se utiliza para tratar el carcinoma urotelial, el cáncer de pulmón de células no pequeñas (CPNM), el cáncer de mama triple negativo (CMT), el cáncer de pulmón de células pequeñas (CPCP) y el carcinoma hepatocelular (CHC). Se trata de un anticuerpo monoclonal totalmente humanizado de isotipo IgG1 contra la proteína ligando de muerte celular programada 1 (PD-L1).
Los efectos secundarios más comunes cuando se utiliza solo incluyen cansancio, disminución del apetito, náuseas (sensación de malestar), vómitos, tos, dificultad para respirar, diarrea, sarpullido, fiebre, dolor en la espalda, las articulaciones, los músculos y los huesos, debilidad, picor e infección del tracto urinario (infección de las estructuras que transportan la orina).
Los efectos secundarios más frecuentes cuando se utiliza con otros medicamentos contra el cáncer son neuropatía periférica (daño nervioso en manos y pies), náuseas, anemia (recuento bajo de glóbulos rojos), neutropenia (recuento bajo de glóbulos blancos), trombocitopenia (recuento bajo de plaquetas), erupción cutánea, cansancio, estreñimiento, disminución del apetito, diarrea y tos.
El atezolizumab es el primer inhibidor de PD-L1 aprobado por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA).
https://en.wikipedia.org/wiki/Atezolizumab
Se aprobó una inmunoterapia adyuvante para algunos pacientes con cáncer de pulmón
La Administración de Alimentos y Medicamentos (FDA) aprobó el medicamento de inmunoterapia atezolizumab (Tecentriq) como tratamiento adyuvante (adicional) después de la cirugía y la quimioterapia para algunos pacientes con cáncer de pulmón de células no pequeñas (CPCNP).
Esta es la primera vez que se aprueba un medicamento de inmunoterapia como tratamiento adyuvante para las personas con cáncer de pulmón.
La aprobación del 15 de octubre es para uso en los pacientes que tienen CPCNP entre los estadios II y IIIA, es decir, con diseminación local (cerca del tumor). Además, los tumores deben expresar la proteína PD-L1 en el 1 % o más de las células tumorales, algo que se determina mediante una prueba aprobada por la FDA. La FDA también aprobó una prueba diagnóstica con fines terapéuticos llamada Ventana PD-L1 (AP263) para identificar a los pacientes que podrían recibir el tratamiento adyuvante con atezolizumab.
La aprobación se basa en los resultados del estudio clínico IMpower010, que incluyó a más de 1000 pacientes con CPCNP a quienes se les extirparon tumores. Todos los pacientes recibieron quimioterapia adyuvante antes de que se les asignara al azar para recibir atezolizumab o cuidado médico de apoyo.
El grupo que recibió atezolizumab adyuvante sobrevivió cerca de 7 meses más, sin recidiva del cáncer y sin que se formara un nuevo cáncer de pulmón (supervivencia sin enfermedad), en comparación con el grupo que recibió cuidados médicos de apoyo.
Las mejoras fueron más notables en los pacientes cuyos tumores tenían concentraciones altas de PD-L1, informaron los investigadores en The Lancet el 20 de septiembre. La PD-L1 es el biomarcador que más se usa para guiar la administración de medicamentos de inmunoterapia llamados inhibidores de puntos de control inmunitario, como el atezolizumab.
https://www.cancer.gov/espanol/noticias/temas-y-relatos-blog/2021/fda-atezolizumab-adyuvante-cancer-pulmon
Disponible en España atezolizumab, la primera inmunoterapia para tratar el cáncer de pulmón microcítico
3 de octubre de 2021
..Redacción.
España cuenta con un nuevo tratamiento para tratar el cáncer de pulmón microcítico (CPM) o de células pequeñas. Se trata del anticuerpo monoclonal antiPD-L1 atezolizumab, comercializado por Roche bajo la marca Tecentriq y que constituye un nuevo avance dentro del esfuerzo investigador.
El CPM es un subtipo de tumor con un crecimiento agresivo y pronóstico desfavorable, para el que no ha habido mejoras en mucho tiempo. Atezolizumab fue el primer fármaco de la familia de inhibidores de PD-L1 en llegar, con una doble indicación para tumores de pulmón no microcítico y urotelial en estados avanzados o metastásicos. Además, España ha participado en el desarrollo clínico de esta terapia, en los estudios IMpower133 e IMfirst, con 36 hospitales y 180 pacientes de diferentes comunidades.
Atezolizumab en combinación con quimioterapia ayuda a los pacientes a vivir significativamente más en comparación con la quimioterapia sola
La autorización se basa en los resultados del estudio fase III IMpower133. Este ha mostrado que atezolizumab en combinación con quimioterapia ayuda a los pacientes a vivir significativamente más en comparación con la quimioterapia sola en la población con intención de tratar (ITT). Esta combinación basada en atezolizumab redujo también significativamente el riesgo de progresión de la enfermedad o muerte (SLP) en comparación con quimioterapia solo.
https://isanidad.com/196881/disponible-en-espana-atezolizumab-la-primera-inmunoterapia-para-tratar-el-cancer-de-pulmon-microcitico/
https://www.roche.es/es_es/comunicacion/actualidad/2021/septiembre/disponible-en-espana-la-primera-inmunoterapia--tecentriq----atez.html
Cáncer de pulmón de células no pequeñas
Cáncer de pulmón de células pequeñas
Cáncer de vejiga
Vídeo:
Visitas: 839
Mostrando Registros desde el 1 hasta el 0 de un total de 0





