Búsqueda
Búsqueda Avanzada
de Fármacos
Anatomía
A tener en cuenta:
- Lista de Carcinógenos por el IARC (Agencia internacional de investigación del cáncer)
- Cáncer y Medio Ambiente por ANSES (Agencia nacional de seguridad sanitaria francesa)
- Oncogenes
- Epigenética y Cáncer
- Resistencia a drogas mediada por la glicoproteína P
- Vacunas terapéuticas en cáncer
- Factores de Crecimiento y Citocinas
- Apoptosis: muerte celular programada
- Receptores de superficie celular
Teoría Básico
Cánceres más visitados
31585
Leucemia linfoblástica aguda
18206
Cáncer tiroideo
16237
Tumor de células germinales extragonadal
15698
Cáncer de vejiga
15087
Fármacos más visitados
30828
Yodo radiactivo (I-131)
20484
Hipertermia magnética por nanopartículas
17457
Denosumab
16842
Bicalutamida
15769
Novedades Fármacos/Tratamientos
Últimos comentarios
Megestrol acetato
Estoy en Búsqueda del medicamento Acetato de Megestrol Muchas gracias Estoy atento a cualquier... Mario
Mesotelioma pleural maligno
Hola José. Lo que le han hecho son tratamientos paliativos porque realmente no tiene cura, puede... Jose
Mesotelioma pleural maligno
Dear Dr. I have afriend with this desease and as far as I know there is contact with asbestos or... Rebeca
Histiocitoma fibroso maligno óseo
Este medicamento funcionaria para un adulto de 86 años. Gracias... NEMESIO
Ciproterona
llevo 9 meses tomando androcur 30 mg.mis senos han crecido siento piquete y se ha despertado el...
Tipo: Inmunoterapias
En este grupo se incluyen todos aquellos medicamentos capaces de estimular el sistema inmune del propio paciente para que éste sea capaz de reconocer y combatir las células enfermas. Algunos expertos los consideran una forma diferente de tratamiento al margen de la quimioterapia. La primera evidencia de 'inmunoterapia' data de finales del siglo XIX, en 1892, cuando William Cloey, un cirujano neoyorquino apreció una regresión espontánea del sarcoma entre aquellos de sus pacientes que habían padecido previamente una infección bacteriana.
Categoría: Inhibidores de los puntos de control inmunitario
Otros tipos de anticuerpos monoclonales mejoran su sistema inmunitario inhibiendo o deteniendo los puntos de control inmunitarios. El organismo utiliza los puntos de control inmunitario para detener de forma natural la respuesta del sistema inmunitario de atacar las células sanas. Las células cancerosas pueden hallar formas de esconderse del sistema inmunitario mediante la activación de estos puntos de control.
Los inhibidores de los puntos de control inmunitario evitan que las células cancerosas bloqueen el sistema inmunitario. Los puntos de control frecuentes que afectan estos inhibidores son las vías PD-1/PD-L1 y CTLA-4.
Diana:PD-1
La muerte celular programada, también conocida como PD-1 y CD279 (grupo de diferenciación 279), es una proteína que en los humanos está codificada por el gen PDCD1. PD-1 es un receptor de superficie celular que pertenece a la superfamilia de las inmunoglobulinas y se expresa en las células T y las células pro-B. PD-1 se une con dos ligandos, PD-L1 y PD-L2.PD-1 y sus ligandos juegan un papel importante en la regulación hacia abajo del sistema inmunológico mediante la prevención de la activación de las células T, que a su vez reduce la autoinmunidad y promueve la auto-tolerancia. El efecto inhibidor de PD-1 se lleva a cabo a través de un doble mecanismo de promoción de la apoptosis (muerte celular programada) en células T antígeno específicas en los ganglios linfáticos al mismo tiempo reduce la apoptosis de las células T reguladoras (células T supresoras).
Una nueva clase de fármacos que bloquean, inhibidores de la PD-1, activan el sistema inmunológico para atacar los tumores y por lo tanto se utilizan para tratar el cáncer.
http://en.wikipedia.org/wiki/Programmed_cell_death_1
La PD-1, del inglés "Programmed Death-1", es una de esas proteínas que hace que nuestro sistema inmune, no elimine a las células tumorales malignas, y por lo tanto el bloqueo de ésta proteina sería una diana con potencial terapéutico para tratar procesos oncológicos. Actualmente se estan desarrollando fármacos contra esta proteína y sus ligandos, y aunque estan en sus fases inciales, es interesante por el posible impacto y potencial control del cáncer (N Engl J Med. 2012). Los anticuerpos dirigidos contra PD-1, producen respuesta en aproximadamente uno de cada 4-5 pacientes con cáncer de pulmón no mícrocítico, melanoma y cáncer renal.
http://oncorred.blogspot.com.es/2012/06/proteina-de-la-muerte-programada-y.html
Nombre:
Nivolumab
Comercial:
Opdivo ®
Estado: Aprobado
Tratamientos aprobados por los diferentes organismos públicos y agencias de regulación sanitarias.
Tecnología: Anticuerpo Monoclonal

Foto:
Fórmula:
Gráfico:
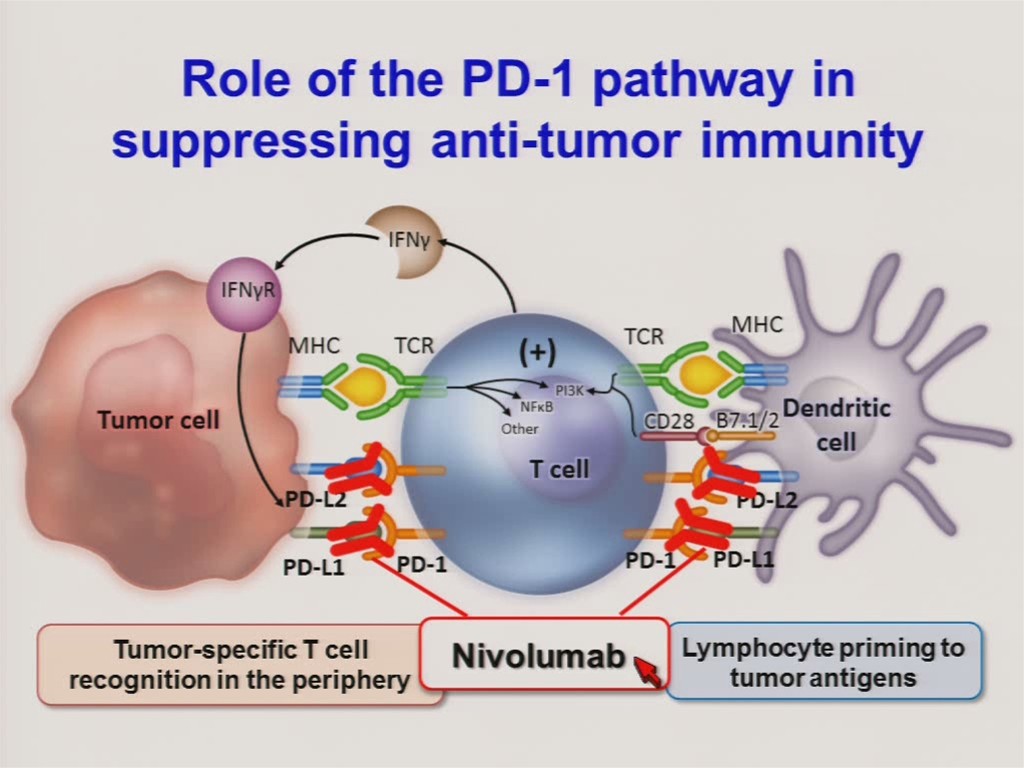
Información: Estados Unidos aprueba nivolumab, un nuevo tratamiento contra el cáncer de pulmón
Ha conseguido un índice de supervivencia global notablemente superior al del docetaxel, con una reducción del 41% del riesgo de muerte
Viernes, 06 de marzo de 2015, a las 17:47
Industria
SEGUNDA APROBACIÓN EN EEUU DE ESTE FÁRMACO
Estados Unidos aprueba nivolumab, un nuevo tratamiento contra el cáncer de pulmón
Ha conseguido un índice de supervivencia global notablemente superior al del docetaxel, con una reducción del 41% del riesgo de muerte
Viernes, 06 de marzo de 2015, a las 17:47
Menea esta noticia en Meneame.net
Bristol-Myers Squibb Company (NYSE: BMY) ha anunciado que la Agencia de Alimentos y Medicamentos (FDA) de los Estados Unidos ha aprobado la inyección de Opdivo® (nivolumab), por vía intravenosa para el tratamiento de pacientes con cáncer de pulmón no microcítico de tipo escamoso metastásico (NSCLC), con progresión de la enfermedad durante la quimioterapia basada en compuestos de platino o después de ésta.
Nivolumab es la primera y única terapia PD-1 (receptor de muerte programada 1) con una supervivencia global demostrada en pacientes con cáncer de pulmón no microcítico de tipo escamoso metastásico que hayan sido tratados anteriormente. Nivolumab ha conseguido un índice de supervivencia global notablemente superior al del docetaxel, con una reducción del 41% del riesgo de muerte (coeficiente de riesgo: 0,59 [95% CI: 0,44, 0,79; p=0,00025]), en un análisis provisional pre-especificado de un ensayo clínico de Fase III. La supervivencia global media fue de 9,2 meses en el grupo tratado con nivolumab (95% CI: 7,3, 13,3) y de 6 meses en el grupo tratado con docetaxel.
“Bristol-Myers Squibb quiere demostrar su compromiso con los pacientes que sufren cáncer de pulmón presentando Opdivo (nivolumab), la primera terapia inmuno-oncológica para pacientes con cáncer de pulmón no microcítico de tipo escamoso metastásico que hayan sido tratados anteriormente”, comenta Lamberto Andreotti, CEO de Bristol-Myers Squibb.
“El cáncer de pulmón es uno de los más diagnosticados y de más elevada mortalidad en los Estados Unidos, por lo que existe una importante necesidad de encontrar tratamientos que mejoren el índice de supervivencia. Estamos muy agradecidos a los pacientes y profesionales de la salud que han colaborado con nosotros para desarrollar un nuevo tratamiento que tiene el potencial de atender a esa necesidad no cubierta", concluye Andreotti.
Se trata de la segunda aprobación en tres meses para nivolumab en los Estados Unidos, y se basa en los resultados de los ensayos CheckMate -017 y CheckMate -063.
Ensayos clínicos
Nivolumab se asocia con reacciones adversas inmunorelacionadas como neumonitis, colitis, hepatitis, nefritis y disfunción renal, hipotiroidismo e hipertiroidismo, otras reacciones adversas, y toxicidad embriofetal.
Un ensayo clínico de Fase III demuestra una supervivencia mayor frente al estándar de CheckMate -017 es un ensayo clínico de Fase III, abierto, aleatorio, multinacional y multicéntrico que ha evaluado el tratamiento con nivolumab (3 mg/kg por vía intravenosa durante 60 minutos cada dos semanas) (n=135) frente al estándar de referencia, docetaxel (75 mg/m2 por vía intravenosa administrado cada 3 semanas) (n=137), en pacientes con cáncer de pulmón no microcítico de tipo escamoso metastásico, con progreso de la enfermedad durante el tratamiento con quimioterapia combinada basada en compuestos de platino o después de ésta.
En este ensayo han participado pacientes independientemente de su estado PD-L1 (ligando 1 de muerte programada). El criterio principal de valoración de este ensayo fue la supervivencia global.
El ensayo se paró el pasado mes de enero después de una evaluación realizada por el Comité de Monitorización de Datos (DMC), órgano independiente que concluyó que el estudio había alcanzado su objetivo, demostrando una supervivencia global superior en pacientes que recibieron nivolumab frente a los que recibieron docetaxel. El análisis provisional pre-especificado se llevó a cabo tras observar 199 casos (el 86% del número de casos previstos para el análisis final) (86 en el grupo de nivolumab y 113 en el grupo de docetaxel).
Nivolumab es la única monoterapia aprobada por la FDA que ha demostrado tener una supervivencia global superior en comparación con el estándar de referencia, en más de 15 años de estudio del cáncer de pulmón no microcítico de tipo escamoso metastásico que haya sido tratado anteriormente. La supervivencia global media fue de 9,2 meses en el grupo tratado con nivolumab (95% CI: 7,3, 13,3) y de 6 meses en el grupo tratado con docetaxel (95% CI: 5,1, 7,3).
El coeficiente de riesgo fue de 0,59 (95% CI: 0,44, 0,79; p=0,00025). Este coeficiente de riesgo significa una reducción del 41% en el riesgo de muerte en pacientes tratados con nivolumab en comparación con el tratamiento con docetaxel.
“La aprobación de Opdivo (nivolumab) por parte de la FDA introduce una modalidad de tratamiento totalmente nueva que ha demostrado unos resultados sin precedentes para el tratamiento del cáncer de pulmón no microcítico de tipo escamoso metastásico que haya sido tratado anteriormente, y que tiene el potencial de sustituir a la quimioterapia para estos pacientes”, afirma el Doctor en Medicina Suresh Ramalingam, Profesor y Director del Medical Oncology, Winship Cancer Institute de la Universidad de Emory. “Este hito es la encarnación de la esperanza largamente sostenida de que los medicamentos inmuno-oncológicos pueden ser notablemente eficaces en estos grupos de pacientes con un tratamiento difícil”.
http://www.redaccionmedica.com/secciones/industria/estados-unidos-aprueba-nivolumab-un-nuevo-tratamiento-contra-el-cancer-de-pulmon-79033
http://en.wikipedia.org/wiki/Nivolumab
http://www.esmo.org/Conferences/Past-Conferences/ESMO-2014-Congress/News-Articles/Results-of-a-Phase-III-Randomised-Study-of-Nivolumab-in-Patients-with-Advanced-Melanoma-After-Prior-Anti-CTLA4-Therapy
Cáncer de pulmón de células no pequeñas
Melanoma
Vídeo:
Visitas: 2433
Mostrando Registros desde el 1 hasta el 0 de un total de 0





